| ~{فعاليات منتديات وهج الذكرى}~ | |
|
 |
|
|
|
أدوات الموضوع | انواع عرض الموضوع |
|
#1
|
|||||||||||
|
|||||||||||
|
قوانين الغازات الغازات gases laws : قوانين لها علاقة بدرجة حرارة و ضغط و حجم الغاز المثالي . يوجد عدد من القوانين فسرت تلك العلاقات و من أهمها : 1 – قانون بويل : في عام 1662 وجد العالم الآيرلندي روبيرت بويل أنه عند ثبوت درجة الحرارة فإن حجم كتلة معينة من الغاز يتناسب عكسيا مع الضغط المؤثر عليه ، أي ن Vα1/P و V=k/P إذا PV=k 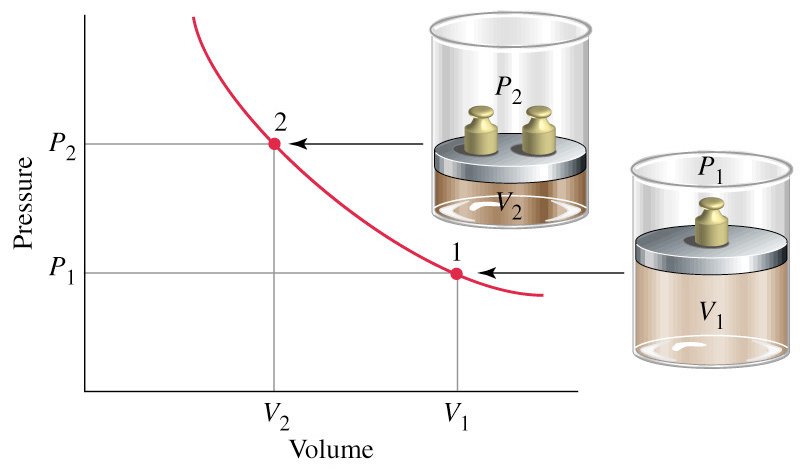 حيث V هو حجم كتلة معينة من الغاز و P الضغط المؤثر على الغاز و k ثابت تعتمد على قيمة و كتلة الغاز ودرجة الحرارة . 2 – قانون شارل : ينص قانون شارل على أنه يتناسب حجم كمية معينة من غاز ما تناسبا طرديا مع درجة حرارته المطلقة تحت ضغط ثابت . 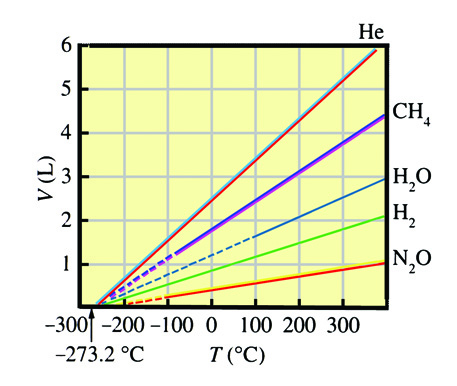 V1/T1 = V2/T2 OR V1/V2 = T1/T2 إذا أطيع قانون شارل بدقة ، فإن الغازات لن تتكثف عندما تبرد . ذلك يعني أن الغازات تتصرف بشكل مثالي عند درجـات حرارة عالية و ضغوط منخفضة نسبيا فقط . 3 – قانون دالتون للضغوط الجزيئية : الضغط الممارس من قبل كل غاز في المزيج يدعى الضـغط الجزيئي . و الضغط الكلي يساوي مجموع الضغوط الجزيئية لكل غاز في المزيـج . و بالإمكان التعبير عن هذه العبارة المعروفة بقانون دالتون للضغوط الجزيئية بالمعادلة التالية : 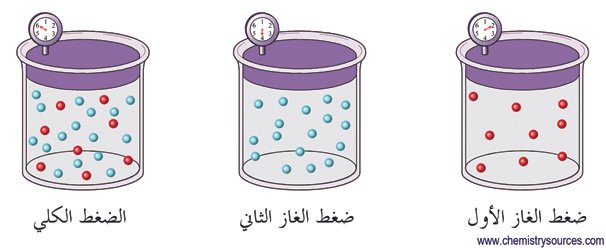 PT = Pa + Pb + Pc+ …….. و عندما يجمع الغاز المحضر في المختبر عن طريق إزاحة الماء ، فإنه يصبح “ملوثا” بجزيئات الماء التي تتبخر إلى داخل الغاز , و بالتالي يساهم ضغط بخار المــاء في الضغط الكلي للغاز الرطب ، و هكذا نستطيع أن نكتب : PT=Pgas+PH2O حيث Pgas ضغط الغاز الجاف و PH2O الضغط البخاري للماء عند درجة حرارة النظام . 4 – قانون غاي لوساك : ينـص قانون غاي لوساك على أن ضغط كمية محددة من الغاز يتناسب طرديا مع درجة حرارته المطلقة إذا ما تم إبقاء حجم الغاز ثابتا . 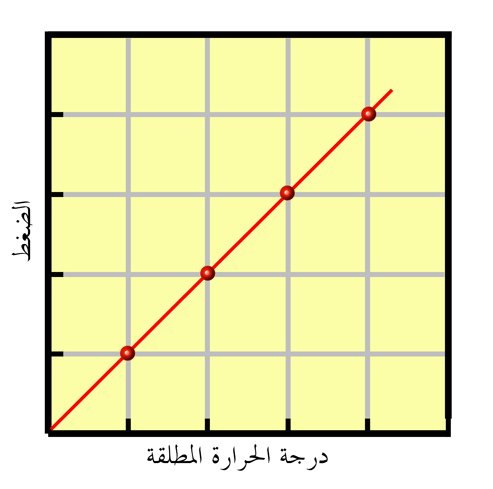 P1/T1=P2/T2 ينص قانون غاي لوساك للحــجوم المتحدة على أن حجوم المواد الغازية التي يتم استهلاكها و إنتاجها في تفاعل كـيميائي تكون في نسب مـكونة مــن أعداد صحيحة صغيرة بشرط أن يتم قياس الأحجام تحت نقس الظروف من درجة الحرارة و الضغط .5 – قانون الغاز المثالي : و هذا القانون يمكن تمثيله بالعلاقة التالية : PV=nRT إن الغازات المثالية الفرضية فقط هي التي تمتثل تماما للنص الرياضـي لقانــون الغاز المثــالي ، و هذا النص يطلق عليه أيضا معادلة الحالة لغاز مثالي . و ذلك لأنها تربط بين تلك المتغيرات ) P,V,n,T ( التي تحدد الخواص الفيزيائية للغاز . و جزيئات الغازات المثالية لا يوجد رابط بيــنها و ليس لها حجم فعــلي لذلك فهي نقاط مجردة . و عندما يقترب غاز حقيقي كثيرا من الامتثال لقانون الغاز المثالي يقال بأن تصرفه مثالي و بالتالي يمكن استعمال قانون الغاز المثالي لوصف تصرفها بدقة معقولة . المواضيع المتشابهه: |
|
|
#3 |
  |
ملاك يارب يستفيدو من المواضيع يا اخي هدفنا هو نشر العلم والمعرفة والتطلع على تاريخنا ومقوماتنا والتعرف على عادتنا المختلفة حتى يكون جسر للتواصل بين كافة الاخوة العرب والمسلمين أجمل وأرق باقات ورودى لردك الجميل ومرورك العطر تحياتي لك كل الود والتقدير دمت برضى من الرحمن لك خالص احترامي .gif) |

|
 |
| كاتب الموضوع | الحسناء | مشاركات | 12 | المشاهدات | 2047 |
 |
|  | |

| انشر الموضوع |
 (عرض التفاصيل)
الأعضاء الذين شاهدوا هذا الموضوع منذ بعد 04-28-2024, 01:43 AM
(إعادة تعين) (حذف)
(عرض التفاصيل)
الأعضاء الذين شاهدوا هذا الموضوع منذ بعد 04-28-2024, 01:43 AM
(إعادة تعين) (حذف)
|
|
| لا توجد أسماء لعرضهـا. |
|
|
الساعة الآن 03:11 PM بتوقيت الرياض
Designed and Developed by : Jinan al.klmah



















 [IMG]http
[IMG]http 





.gif)

















 العرض العادي
العرض العادي